הקדמה
שימוש בתרופות בהנקה הוא תחום טיפולי שעלול להיות מרתיע עבור רוב אנשי הצוות הרפואי שאינם עוסקים בו באופן יומיומי. הסיבות העיקריות לכך הן:
- בטיחות – ההבנה כי מדובר הלכה למעשה בשני מטופלים, אשר רק אחד מהם (האם) זקוק לתרופה, יוצרת חשש מפני תופעות לוואי ברמות חומרה שונות (ולכאורה בלתי-צפויות) אצל התינוק. יילודים ותינוקות הינם ממילא אוכלוסיה רגישה, והעובדה שתינוק בריא (ועל אחת כמה וכמה תינוק חולה) עלול להיחשף לתרופה שאיננו זקוק לה מעלה חששות רבים אצל המטפלים באם המניקה.
- חוסר ניסיון בתחום – מדובר בתחום התמחות ספציפי, אשר דורש הבנה בפיזיולוגיה של ההנקה, בפרמקוקינטיקה וברפואת ילדים, שהינה תחום מורכב כשלעצמו ובעל מאפיינים ייחודיים (זהו התחום היחידי ברפואה שבו המטופל יכול להכפיל או אף לשלש את משקלו תוך מספר חודשים!).
שתי הנקודות שלעיל כמובן מתארות בצורה נכונה את המורכבות של התחום, אבל האם הן אכן מצדיקות הימנעות של אנשי צוות רפואי, ובפרט רוקחים, מנגיעה בתחום זה והסתמכות על מומחים בלבד? התשובה היא לא, משלוש סיבות:
- שאלות על שימוש בתרופות בהנקה יכולות לצוץ בכל עת, בין אם בעבודה או בחיים האישיים, והמומחים בתחום זה, שנמצאים במרכזי הייעוץ השונים ברחבי הארץ (ר’ רשימה בהמשך) ועושים שם את עבודתם החשובה, אינם זמינים בכל עת למענה.
- תחום השימוש בתרופות בהנקה – לעומת שימוש בתרופות בהיריון – נסמך ברובו על עקרונות פרמקוקינטיים פשוטים, שהיכרות איתם יכולה לתת לכל אחד יכולת להסיק מסקנות ולקבל החלטות מושכלות לגבי בטיחות השימוש בתרופה אצל אישה מניקה, לפחות ברמה של מענה ראשוני עד להתייעצות עם מומחה.
- ישנם מקרים אקוטיים שבהם האישה המניקה צריכה לקחת תרופה וזקוקה להכוונה. ייעוץ לא נכון או אי מתן ייעוץ כלל עלול לפגוע ביעילות הטיפול של האישה, להזיק לתינוק או להזיק להנקה (בפרט בימים הראשונים לאחר הלידה). הכוונה נכונה, גם אם אינה נותנת מענה לתמונה בכללותה, תביא תועלת ותמזער את הסיכון לכל אחד מהם.
מטרת הפוסט הזה היא לפרוש את העקרונות הפרמקוקינטיים העומדים בבסיס הייעוץ התרופתי לנשים מניקות, במטרה לאפשר לכל קורא להבין כיצד ניתן לקבל החלטה מושכלת לגבי שאלות בתחום זה.
הערה חשובה: פוסט זה איננו מתיימר ואיננו מסוגל להחליף פניה לאחד ממרכזי הייעוץ התרופתי המוסמכים. למומחים בתחום זה ישנה היכולת לתת תשובות מוסמכות ומלאות ככל שניתן על סמך מקורות מידע ספציפיים, היכרות עם מחקרים עדכניים, מחקרים מקוריים וניסיון רב-שנים (זה המקום להוקיר את פועלם ולהעריך את תרומתם הרבה בקליניקה ובאקדמיה. גילוי נאות: כותב שורות אלו נמנה בעבר על צוותו של פרופ’ מתי ברקוביץ’ ביחידה לפרמקולוגיה קלינית וטוקסיקולוגיה במרכז הרפואי “שמיר”).
הכוונה בפוסט היא לתת כלים ל”עזרה ראשונה” למטופלת, עד שניתן יהיה להתייעץ עם מומחה.
הפיזיולוגיה של ההנקה ונקודות חשובות לגבי תרופות בחלב אם
חלב אם מתחיל להיווצר סביב אמצע תקופת ההיריון, עם התפתחות השד והפיכתו – תחת ויסות הורמונלי הדוק – מ-‘עץ צינוריות פשוט’ לאיבר אקסוקריני (מפריש) יעיל ביותר. בועיות/אוניות (lobules) החלב הן מבנים דמויי-כיס אשר מהווים צבר של “שקיקי חלב” (alveoli), ששכבת התאים הלומינלית שלהם מורכבת מתאים מיוחדים הנקראים לקטוציטים, אשר מפרישים לחלל השקיק חומרים שונים שיוצרים יחד את חלב האם (ר’ איור 1). חלק מהחומרים הם מומסים אנדוגניים, קרי, מגיעים מהציטופלסמה של הלקטוציטים עצמם ומופרשים לחלב בתהליך של אקסוציטוזה (מסלול I), כגון מים, לקטוז, אוליגוסכרידים, פוספאט, סידן וציטראט, וכן ליפידים שמופרשים כטיפות שומן אל החלב (מסלול II). לעומת זאת, חלק מהחומרים הינם חומרים אקסוגניים, כלומר, מגיעים ממקום אחר בגוף דרך פלסמת הדם. חומרים אלו מגיעים אל החלב במנגנונים טרנסצלולריים (מעבר דרך התא) או פאראצלולריים (מעבר בין התאים).
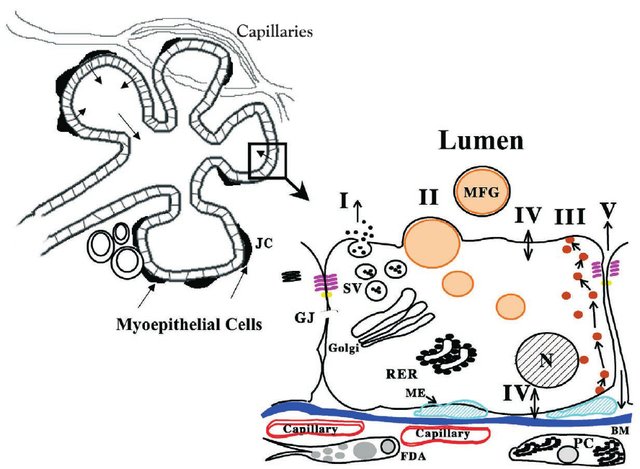
משמאל: תרשים של מבנה שקיק החלב. השכבה הלומינלית מורכבת מלקטוציטים שמפרישים את מרכיבי החלב אל חלל השקיק.
מימין: תרשים מוגדל של לקטוציט עם המסלולים השונים למעבר חומרים אל חלב אם:
I – אקסוציטוזה של חומרים אנדוגניים מתוך התא
II – הפרשת טיפות שומן מתוך התא כבועיות עטופות ממברנה (“פינוציטוזה הפוכה”)
III – מסלול טרנסצלולרי של מולקולות גדולות כגון חלבונים בתוך בועיות מהחלל הבין-תאי אל חלל שקיק החלב
IV – מסלול טרנסצלולרי של יונים ומולקולות קטנות דרך טרנספורטרים ממברנליים, גם בצד הבזאלי וגם בצד האפיקלי
V – מסלול פאראצלולרי אשר מתאפשר הודות למרווחים יחסית גדולים בין הלקטוציטים. קיים רק במצב של היריון, בימים הראשונים לאחר הלידה ובמצבי דלקת בשד
קיצורים:
SV, secretory vesicle; RER, rough endoplasmic reticulum; BM, basement membrane; N, nucleus; PC, plasma cell; FDA, fat depleted adipocyte; JC, junctional complex containing the tight and adherens junctions; GJ, gap junction; ME, myoepithelial cell.
מתוך: Neville, 1999
מעבר דרך התא מיועד למולקולות גדולות יחסית (מסלול III), כגון חלבוני פלסמה (אלבומין, טרנספרין), הורמונים אנדוקריניים (אינסולין, פרולקטין, אסטרוגן) וציטוקינים. חומרים אלו נבלעים על ידי התא בתהליך של אנדוציטוזה דרך ממברנת הבסיס הקרובה לנימי הדם הצמודים לשקיקים, ומופרשים אל חלל השקיק דרך הצד האפיקלי של הלקטוציטים. בממברנת הלקטוציטים גם קיימים טרנספורטרים שונים (מסלול IV), אשר מאפשרים מעבר של יונים ומולקולות קטנות כגון גלוקוז וחומצות אמינו מהצד הבזאלי אל הצד האפיקלי.
המעבר הפאראצלולרי (בין התאים) הוא מסלול שמאפשר מעבר ישיר של חומרים מהנוזל הבין-תאי אל שקיק החלב (מסלול V). בדרך כלל, מסלול זה אינו קיים מכיוון שהלקטוציטים צמודים זה לזה, אולם בימים הראשונים לאחר הלידה (או במצב של דלקת בשד), נוצרים מרווחים בין הלקטוציטים על מנת לאפשר מעבר מהיר וקל של חומרים חשובים וגדולים יחסית, כגון תאי מערכת החיסון (מקרופאגים, נויטרופילים, לימפוציטים) ונוגדנים שונים. במהלך השבוע הראשון לאחר הלידה, הלקטוציטים מתנפחים תחת השפעת פרולקטין, והמרווחים הבין-תאיים נסגרים.
תרופות יכולות לעבור מהפלסמה אל חלב האם במנגנון טרנסצלולרי או פאראצלולרי בדיוק כמו החומרים האנדוגניים הנזכרים לעיל, ולפי אותם מאפיינים, כלומר: תרופות בעלות משקל מולקולרי נמוך, תרופות הידרופוביות, תרופות שיכולות להוות סובסטרט לטרנספורטרים שונים יכולות לעבור מהפלסמה אל החלב במסלול טרנסצלולרי, אקטיבי או פסיבי, ותרופות בעלות משקל מולקולרי גבוה יחסית, כולל חלבונים, יכולות לעבור במסלול הפאראצלולרי – אם הן נמצאות בפלסמה בימים הראשונים לאחר הלידה (חשוב במיוחד עבור נשים שמטופלות באופן קבוע בתרופות ביולוגיות המכילות נוגדנים).
על אף האפשרות למעבר של תרופות לחלב אם, יש לזכור שני עקרונות חשובים:
- חלב אם הינו המזון הטוב ביותר עבור התינוק. כלל רשויות וגופי הבריאות מסכימים על כך.
- הספרות הרפואית העדכנית מראה שרק מעט תרופות באופן יחסי עוברות לחלב אם במידה כזו שעלולה לסכן את התינוק באופן משמעותי מבחינה קלינית.
לפיכך, בעת ייעוץ לגבי טיפול תרופתי בהנקה, חשוב לבדוק היטב את המידע הקיים לגבי התרופה ולבדוק סיכון מול תועלת (ברוב המקרים התועלת תעלה על הסיכון), ולעשות כל מה שניתן כדי לשמר את ההנקה אצל אמהות שרוצות בכך, בפרט בימים הראשונים לאחר הלידה שהינם קריטיים לביסוס הנקה. המלצה לא להניק צריכה להיות מוצא אחרון, ועדיף שתעשה לאחר התייעצות עם מומחה בתחום.
פרמטרים פרמקוקינטיים חשובים להערכת מידת המעבר של תרופה לחלב אם
רוב התרופות עוברות לחלב אם באמצעות דיפוזיה פסיבית, כלומר, בהתאם למפל ריכוזים. זו הסיבה לכך שתרופות עוברות מהפלסמה לחלב אם מלכתחילה – כאשר הריכוז בפלסמה גבוה ובחלב הוא נמוך, התרופה תעבור מהפלסמה אל החלב, עד שריכוזה בפלסמה יתחיל לרדת בעקבות תהליכי פינוי, וכתוצאה מכך, גם התרופה שבחלב תתחיל לעבור בחזרה אל הפלסמה לפי מפל הריכוזים שהתהפך, ומשם תתפנה מהגוף גם כן. מכיוון שחלב האם מהווה למעשה מדור פרמקוקינטי נוסף בגוף, פרופיל הריכוזים בחלב לרוב מציג מגמה דומה לזו של פרופיל הריכוזים בפלסמה (ר’ איור 2), וניתן להתייחס גם אליו לפי פרמטרים פרמקוקינטיים בסיסיים.
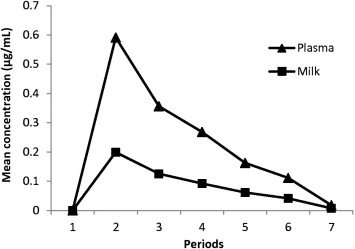
חשוב לציין שהפרמטרים הפרמקוקינטיים של התרופה נותנים מושג בסיסי לגבי ההתנהגות של התרופה בגוף, אולם מדובר בתמונה תיאורטית שבמקרים מסויימים איננה מתארת בצורה מדוייקת את המציאות. בנוסף, אף פרמטר אינו עומד לבדו ואף פרמטר אינו פרמטר מכריע. בחינת ההתאמה של תרופה מסויימת להנקה או השוואה בין מספר תרופות לצורך החלטה איזו מהן עדיפה בהנקה צריכה לקחת בחשבון את התמונה המלאה המצטיירת מהפרמקוקינטיקה של התרופה ומהפרטים הידועים על השפעתה הקלינית על תינוקות בשלבי התפתחות שונים, על מנת לקבל החלטה מושכלת לגבי התאמה או עדיפות של תרופה מסויימת בהנקה. לדוגמא, האנטיביוטיקה Sulfamethoxazole-Trimethoprim אינה מומלצת בהנקה בגלל הפרמקוקינטיקה שלה, אך גם בגלל שהיא עלולה לגרום להיפרבילירובינמיה ביילוד יונק על רקע דחיקת בילירובין שקשור לאלבומין והפיכתו לבילירובין חופשי – תופעה זו אינה מוסברת על ידי הפרמקוקינטיקה של התרופה.
לכן, בעת בחינת הספרות הקיימת לגבי ההתנהגות של תרופה מסויימת בחלב אם מומלץ לעיין במאגרי מידע או ספרים שמציגים פרמטרים פרמקוקינטיים ו/או מאגדים נתונים ממחקרים, כגון ספרו של Hale ומאגר המידע Lactmed (ר’ רשימת מקורות), ולעיתים כדאי גם לחפש באופן ישיר מחקרים פרמקוקינטיים ופרמקודינמיים בחלב אם, כמו המחקר שממנו לקוח האיור שלעיל, שכן מחקרים כאלו מהווים את הכלי הטוב והמדוייק ביותר לתיאור ההתנהגות של תרופה בחלב אם.
זמן מחצית חיים (t1/2)
זמן מחצית החיים (של פינוי) הוא פרמטר פרמקוקינטי בסיסי ומוכר היטב. הוא מתאר את פרק הזמן הדרוש לריכוז התרופה בפלסמה של האם לרדת ב-50%. ככל שזמן מחצית החיים של התרופה קצר יותר, כך היא מתפנה מהר יותר מהגוף והמעבר לחלב נמוך יותר, כך שהחשיפה של התינוק לתרופה קטנה יותר. בשל כך, יש להעדיף עבור נשים מניקות תרופות בעלות זמן מחצית חיים קצר (מספר שעות). מנגד, תרופות בעלות זמן מחצית חיים קצר לרוב מצריכות משטר מינון של 3-4 מנות ביום, מה שעלול להקשות על היענות מיטבית לטיפול, ויש לקחת זאת בחשבון. חשוב לציין שתרופות עם זמן מחצית חיים ארוך יותר אינן בהכרח בעייתיות, ויש לקחת בחשבון את שאר הפרמטרים כדי לקבל תמונה טובה יותר של החשיפה הצפויה לתינוק.
נפח פיזור (Vd)
נפח הפיזור של התרופה גם הוא פרמטר פרמקוקינטי מוכר, אשר מתאר את מידת הפיזור של התרופה בגוף. תרופות בעלות נפח פיזור גדול תהיינה בעלות ריכוז נמוך בדם (![]() ), ולרוב המשמעות היא ריכוז נמוך שלהן בחלב (למעט מקרים של יחס פלסמה/חלב גבוה, ר’ בהמשך). לכן יש להעדיף בהנקה תרופות בעלות נפח פיזור גדול. חשוב לזכור שזמן מחצית חיים הוא פונקציה של נפח הפיזור
), ולרוב המשמעות היא ריכוז נמוך שלהן בחלב (למעט מקרים של יחס פלסמה/חלב גבוה, ר’ בהמשך). לכן יש להעדיף בהנקה תרופות בעלות נפח פיזור גדול. חשוב לזכור שזמן מחצית חיים הוא פונקציה של נפח הפיזור
(![]() ), ולכן ייתכן זמן מחצית חיים ארוך לפינוי מהמדור הפריפראלי, ובו בעת זמן מחצית חיים קצר לפינוי מהפלסמה. בנוסף, פינוי מהמדור הפריפראלי הינו למעשה חזרה של התרופה מהרקמות אל הפלסמה, ומשם פינוי מהגוף דרך איברי הפינוי (כבד/כליות), וחזרה לפלסמה עלולה להשיב את התרופה גם אל חלב האם במידה מסויימת. לכן נפח הפיזור כשלעצמו אינו מהווה פרמטר ברור שלפיו ניתן לחזות התנהגות של תרופה בחלב אם, אולם ככלל, תרופות בעלות נפח פיזור גדול אמורות להופיע בחלב אם בריכוזים יחסית נמוכים.
), ולכן ייתכן זמן מחצית חיים ארוך לפינוי מהמדור הפריפראלי, ובו בעת זמן מחצית חיים קצר לפינוי מהפלסמה. בנוסף, פינוי מהמדור הפריפראלי הינו למעשה חזרה של התרופה מהרקמות אל הפלסמה, ומשם פינוי מהגוף דרך איברי הפינוי (כבד/כליות), וחזרה לפלסמה עלולה להשיב את התרופה גם אל חלב האם במידה מסויימת. לכן נפח הפיזור כשלעצמו אינו מהווה פרמטר ברור שלפיו ניתן לחזות התנהגות של תרופה בחלב אם, אולם ככלל, תרופות בעלות נפח פיזור גדול אמורות להופיע בחלב אם בריכוזים יחסית נמוכים.
זמן הגעה לריכוז מקסימלי (Tmax = time to Cmax)
זהו פרק הזמן בין מועד נטילת התרופה לבין הגעתה לריכוז המקסימלי (Cmax) בפלסמה, כאשר במקביל היא מגיעה לריכוזה המקסימלי בחלב. מומלץ שלא להניק בתוך פרק הזמן שמהווה את ה-Tmax, מכיוון שזהו פרק הזמן שבו הריכוזים בחלב אם הולכים ועולים. מנגד, לאחר שחלף Tmax הריכוזים בחלב הולכים ויורדים לפי זמן מחצית החיים, והנקה בשלב זה תביא לחשיפה נמוכה יותר של התינוק לתרופה. יש לנסות למצוא את נקודת הזמן האופטימלית להנקה, כך שהתינוק יאכל בזמן הנכון עבורו ובנקודה הרחוקה ביותר האפשרית מה-Tmax.
משקל מולקולרי (MW)
המשקל המולקולרי של התרופה משפיע על האופן שבו היא יכולה (אם בכלל) לעבור מהפלסמה אל החלב. ככל שהמולקולה קטנה יותר, כך קל לה יותר לחצות ממברנות ולעבור מהפלסמה אל החלב. לכן, מולקולות הידרופיליות במשקל נמוך מ-200 Da (למשל, אתנול) עוברות לחלב במידה רבה. מולקולות עד משקל של 800-1000 Da צפויות לעבור אל חלב האם במידה שעשויה להיות משמעותית (בעיקר אם הן מספיק הידרופוביות כדי לחצות ממברנות מבלי להיתקע בהן), אולם תרופות בעלות משקלים מולקולריים גבוהים יותר (כגון חלבונים) לרוב תופענה בחלב רק בכמויות קטנות, אם בכלל.
יחס חלב/פלסמה (M/P)
נתון זה מציין את היחס בין ריכוז התרופה בחלב אם לריכוז התרופה בפלסמה. יחס של 1 מציין כמובן ריכוזים שווים בין החלב והפלסמה, בעוד שיחס גבוה מ-1 מעיד על כך שהתרופה מתרכזת בחלב לעומת הפלסמה ויחס קטן מ-1 מעיד על ריכוז נמוך בחלב לעומת הפלסמה. ככלל, המצב האחרון הוא המועדף, אולם חשוב לזכור שמדובר ביחס, ולכן הוא חסר משמעות ללא נתונים לגבי הרמה האבסולוטית של התרופה בפלסמה, שכן ייתכנו מצבים שבהם יחס חלב/פלסמה הוא גבוה, אבל רמות התרופה בפלסמה נמוכות, כך שבפועל גם הרמות בחלב עשויות להיות מתחת לסף ההשפעה הקלינית על התינוק, גם אם הן גבוהות יותר מהרמות בפלסמה. זהו נתון עזר שנגזר ממחקרים פרמקוקינטיים ולא פרמטר פרמקוקינטי טהור, אולם הוא יכול לסייע להערכה מהירה של הרמות הצפויות בחלב אם.
קישור לחלבונים (PB)
קישור לחלבונים מעיד על אחוז הקישור של התרופה לחלבוני הפלסמה ובראשם אלבומין. מכיוון שתרופות שקשורות לחלבונים לא יכולות לחצות ממברנות, ככל שאחוז הקישור גבוה יותר, כך הכמות החופשית למעבר לחלב נמוכה יותר, ולכן ככלל יש להעדיף תרופות בעלות אחוז קישור גבוה לחלבונים (מעל 90%).
זמינות ביולוגית (Bioavailability)
הזמינות הביולוגית הינה מדד לכמות התרופה שמגיעה בפועל לפלסמה של האם מתוך המנה שניטלה דרך הפה, לדוגמא, המשמעות של זמינות ביולוגית של 50%, היא שרק חצי מהמנה שניטלה הגיעה בפועל לפלסמה (ישנן סיבות שונות לכך, כגון ספיגה נמוכה בדופן מערכת העיכול, First pass metabolism בכבד, הרס בסביבה החומצית של הקיבה ועוד).
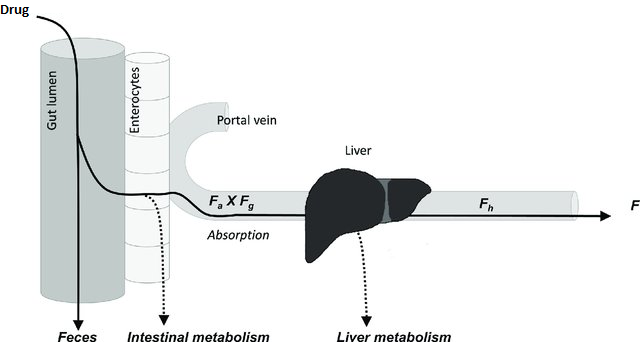
Fa – הפרקציה של המנה שלא התפרקה בקיבה או יצאה בצואה
Fg – הפרקציה של המנה שהצליחה לחצות את דופן המעי
Fh – הפרקציה של המנה שלא עברה First pass metabolism בכבד
מכפלת הפרקציות הנ”ל נותנת את הפרקציה הסופית שהגיעה לפלסמה מתוך המנה שניטלה
לרוב, ערכי הזמינות הביולוגית שמופיעים בספרות מצויינים עבור מטופלים מבוגרים, אולם הם יכולים לתת מושג לגבי מידת הספיגה של התרופה גם אצל תינוקות (אם כי יש להיזהר בפרשנות במקרים של תינוקות פגים או צעירים מאוד עקב תפקוד כבדי מופחת, קיבה פחות חומצית, ספיגה משתנה דרך דופן מערכת העיכול וכו’). ככלל, ההעדפה היא לתת לאם תרופות בעלות זמינות ביולוגית נמוכה.
בנוסף, יש לזכור שהחשיפה של התינוק לתרופה שנמצאת בחלב היא תמיד פומית, ללא קשר לדרך המתן אצל האם. כלומר, גם תרופות שניתנות לאם דרך הווריד (שבדרך כלל ניתנות כך עקב זמינות ביולוגית נמוכה) מגיעות אל התינוק דרך הפה ועוברות בקיבה, שם לרוב הן מתפרקות, או שהן מגיעות לכבד ועוברות שם First pass metabolism משמעותי.
pKa
ה-pKa של התרופה הוא ה-pH שבו 50% מהתרופה מיוננים ו-50% אינם מיוננים. ככל שהתרופה יותר מיוננת, כך יכולתה לחצות ממברנות נמוכה יותר, ולכן המעבר מהפלסמה לחלב אם יהיה נמוך יותר. מכיוון שחלב אם מעט יותר חומצי מהפלסמה (pH של 7.2 לעומת 7.35-7.45, בהתאמה), תרופות שהינן בסיסים חלשים (pKa בין 7 ל-10) מתייננות במידה רבה יותר עם כניסתן לחלב ועלולות להיתקע שם בכמות גדולה יותר לעומת הכמות בפלסמה (תופעה הנקראת ion trapping). לתרופות מהסוג הזה גם צפוי שיהיה יחס חלב/פלסמה יחסית גבוה. לכן, ההעדפה בהנקה היא לתרופות עם pKa נמוך, מכיוון שתרופות אלו תהיינה ברובן במצב מיונן ב-pH של הדם, והמעבר שלהן לחלב אם יהיה נמוך יותר.
המנה היחסית של התינוק (RID = Relative Infant Dose)
זהו ערך מחושב באחוזים, אשר מתקבל מחלוקת כמות התרופה שמגיעה אל התינוק במ”ג/ק”ג/יום בכמות התרופה שמקבלת האם במ”ג/ק”ג/יום, כלומר:
![]()
את כמות התרופה שמגיעה לתינוק ניתן לחשב באופן הבא:
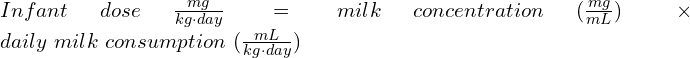
כאשר לרוב ניתן להשתמש בהנחת צריכת חלב יומית סטנדרטית של 150 מ”ל/ק”ג/יום. ה-RID מהווה מדד נוח לחישוב הפרקציה שמגיעה לתינוק מתוך המנה שנטלה האם, ויש להשוותו למינון המקובל בילדים של אותה תרופה (אם קיים), על מנת לראות האם מידת החשיפה גבוהה ביחס לטיפול המקובל בתרופה בתינוקות. עם זאת, יש לציין ש-RID לא מספק מידע לגבי רעילות ותופעות לוואי אצל התינוק. ככלל, ההעדפה היא לתת תרופות בעלות % RID < 10.
מקורות מידע לפרמטרים פרמקוקינטיים ופיזיקו-כימיים
- עלונים לרופא במאגר התרופות של משרד הבריאות
- PubChem – מאגר מידע פתוח לכל המכיל מונוגרפים מפורטים של תרופות וחומרים כימיים אחרים, מבית ה-NIH.
- DrugBank – מאגר מידע פרמקולוגי קנדי, פתוח לכל. מכיל נתונים פרמקולוגיים, כימיים ועוד.
- HalesMeds.com – הגרסה האלקטרונית של ספרו של ד”ר תומאס הייל – Hale’s Medications & Mothers’ Milk. מאגר המידע מתוחזק ומעודכן מעת לעת, אולם גישה אליו דורשת מנוי בתשלום.
נקודות נוספות שמומלץ לקחת בחשבון
- האם לתרופה ישנו מטבוליט פעיל? מהו זמן מחצית החיים שלו במבוגרים ובילדים?
מטבוליטים פעילים בעלי זמן מחצית חיים ארוך עלולים להצטבר אצל ילדים ולגרום לרעילות. - האם התרופה חודרת את מחסום הדם-מוח?
תרופות שפועלות במערכת העצבים המרכזית מתאפיינות במבנים הידרופוביים ובמעבר יחסית קל דרך ממברנות, ולכן הן לרוב עוברות בקלות מהפלסמה אל החלב במסלול טרנסצלולרי. - בן כמה התינוק ומה מצבו הקליני? האם הוא פג או שנולד בזמן? באיזו רמה הכבד והכליות שלו מתפקדים?
תינוק קטן ו/או חולה עלול להיות פגיע יותר לתרופות, גם אם הכמות בחלב יחסית נמוכה. במצב כזה כמובן חשוב לערב בדיון גם רופא ילדים. - מה היקף ההנקה? האם מלאה או חלקית?
החשיפה של תינוק גדול בהנקה חלקית לתרופות בחלב אם נמוכה יותר באופן יחסי וקל יותר להתאים את מועדי ההנקה לזמני נטילת התרופה, לעומת תינוק קטן בהנקה מלאה. - האם התרופה משפיעה על טעם החלב?
ישנן תרופות שיכולות לשנות את הטעם של החלב לרעה ובכך לפגוע בהנקה, גם אם הן אינן מזיקות לתינוק באופן ישיר. כדאי לבדוק זאת מראש, או להנחות את האם לשים לב לשינויים ברצון של התינוק לינוק. ר’ רשימה מקובלת להלן:
דוגמא יישומית (או: איך הכל מתחבר יחד)
(מתוך Kelsey, 2016)
אישה בת 32 במשקל 78 ק”ג שסובלת מדיכאון טופלה לפני ההיריון בתרופה מקבוצת מעכבי MAO, אולם התרופה הופסקה במהלך השבועות הראשונים להיריון. היא ילדה לפני כ-3 חודשים וכעת רוצה להתחיל שוב טיפול בתרופה נגד דיכאון. הרופא שלה חושב שתרופה מקבוצת ה-SSRIs תתאים יותר מהתרופה שטופלה בה בעבר ומבקש עזרה בבחירת התרופה הטובה ביותר עבורה מקבוצה זו, שכן היא מניקה את בנה (שוקל 6 ק”ג).
מספר נתונים פרמקוקינטיים של כמה תרופות מקבוצת ה-SSRIs מופיעים בטבלה שלהלן:
| שם התרופה | משקל מולקולרי (Da) | זמן מחצית חיים (שעות) | נפח פיזור (ליטר/ק”ג) | זמינות ביולוגית (%) | קישור לחלבונים (%) |
| Citalopram | 405 | 36 | 12 | 80 | 80 |
| Escitalopram | 414 | 27-32 | 20 | 80 | 56 |
| Fluoxetine | 345 | 48-72 | 12-43 | 100 | 94.5 |
| Paroxetine | 329 | 21 | 3-28 | מלאה | 95 |
| Sertraline | 306 | 26 | 20 | מלאה | 98 |
משקל מולקולרי – כל התרופות בעלות משקל מולקולרי יחסית דומה, וכולן יכולות לעבור לחלב אם במידה מסויימת, מכיוון שמשקלן נמוך מ-800 Da.
זמן מחצית חיים – לפלואוקסטין זמן מחצית חיים ארוך משמעותית מהתרופות האחרות ולפארוקסטין הקצר ביותר. עם זאת הוא לא שונה משמעותית מהתרופות האחרות וקרוב ל-24 שעות, כך שגם מבחינת זמן מחצית החיים אין העדפה ברורה לתרופה מסויימת.
נפח פיזור – בחלק מהתרופות קיים טווח די רחב בנפח הפיזור וקשה להעריך כיצד התרופה תתנהג דווקא אצל המטופלת הנדונה. לסרטראלין ואסציטלופרם ישנו נפח פיזור גבוה יחסית לתרופות האחרות וזו תכונה מועדפת, מכיוון שהריכוז בפלסמה והמעבר לחלב אם צפויים להיות נמוכים לעומת תרופות עם נפח פיזור קטן יותר.
זמינות ביולוגית – נמוכה יותר אצל ציטלופרם ואסציטלופרם, אך די גבוהה באופן יחסי עבור כל חמש התרופות ואין תרופה אחת שמתבלטת על רקע זמינות ביולוגית נמוכה משמעותית.
קישור לחלבונים – הערכים הנמוכים יחסית של ציטלופרם ואסציטלופרם בקטגוריה זו מעידים על ריכוז גבוה של תרופה חופשית בפלסמה של האם, לעומת התרופות האחרות, ומנגד, הערך הגבוה ביותר הוא של סרטרלין, כלומר, זו התרופה הכי פחות זמינה למעבר לחלב אם מבין חמש התרופות.
על כן, בשקלול של כל הפרמטרים הנ”ל, נראה שהתרופה המועדפת מבחינה פרמקוקינטית בהנקה היא סרטרלין, בעיקר בשל נפח פיזור גבוה וקישור גבוה לחלבונים.
לחישוב RID, יש להשתמש בריכוז התרופה בחלב מהספרות. הערך הגבוה ביותר שדווח עבור ריכוז סרטרלין בחלב אם הינו ![]() , תחת מינון אמהי של 100 מ”ג/יום. אם התינוק צורך כ-150 מ”ג/ק”ג/יום, מדובר על 900 מ”ל חלב אם ליום (משקל התינוק: 6 ק”ג). לכן, הכמות הכוללת של סרטרלין שמגיעה לתינוק ביום היא:
, תחת מינון אמהי של 100 מ”ג/יום. אם התינוק צורך כ-150 מ”ג/ק”ג/יום, מדובר על 900 מ”ל חלב אם ליום (משקל התינוק: 6 ק”ג). לכן, הכמות הכוללת של סרטרלין שמגיעה לתינוק ביום היא:![]()
כדי לקבל את המינון פר ק”ג משקל גוף של התינוק, יש לחלק במשקל ומתקבל מינון של: ![]()
במינון אמהי של 100 מ”ג/יום, המינון לפי משקל גוף של האם הוא: ![]()
כעת ניתן לחשב RID באופן הבא:
![]()
וכאמור, RID נמוך מ-10% נחשב בטוח עבור התינוק מבחינת חשיפה לתרופה (כמובן שתמיד רצוי להדריך את האם לגבי מעקב אחר התינוק ותגובתו לטיפול).
הרופא המטפל של המטופלת שומע על תרופה חדשה נגד דיכאון ומעוניין לבדוק האם היא עדיפה עבור המטופלת מבחינת בטיחות בהנקה. אין הרבה מידע בספרות על הבטיחות של התרופה החדשה בנשים מניקות, אולם ידועים הנתונים הבאים:
משקל מולקולרי – 730 Da
נפח פיזור – 15 ליטר/ק”ג
קישור לחלבונים – 98%
זמינות ביולוגית – 50%
ריכוז ממוצע בפלסמה במבוגרים – 26 ננוגרם/מ”ל בעקבות מנה של 60 מ”ג/יום
M/P (יחס חלב/פלסמה) – 2
בעזרת הנתונים הללו, ניתן לחשב את החשיפה של התינוק לתרופה ולהעריך את מידת בטיחותה בהנקה:
בהנחה שריכוז התרופה בפלסמה של האם הוא 26 ננוגרם/מ”ל, ריכוז התרופה בחלב אם צפוי להיות:
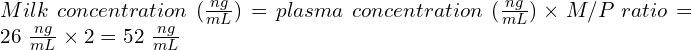
בהנחה שהתינוק יקבל 900 מ”ל חלב אם ביום (לפי 150 מ”ל/ק”ג), כמות התרופה בנפח זה הינה:
![]()
מידת החשיפה של התינוק לתרופה תלויה בזמינות הביולוגית שלה. נתונה זמינות ביולוגית של 50% במבוגרים. אמנם ייתכן שהתינוק יספוג כמות גדולה יותר, אולם בהעדר מידע ספציפי לגבי ספיגה בתינוקות, יש להשתמש בנתון הקיים עבור מבוגרים כדי לקבל בכל זאת מושג לגבי מידת הספיגה של התרופה ממערכת העיכול אל הפלסמה. לפיכך, בהינתן זמינות ביולוגית של 50%, מתוך 47 מק”ג ליום, התינוק צפוי להיחשף לכ-23.5 מק”ג מהתרופה.
כעת, כדי לחשב את ה-RID של התרופה, יש לחשב את המינון היומי לק”ג של התינוק ושל הילד. בהמשך לאמור לעיל, המינון היומי של הילד לק”ג משקל גוף יהיה:
![]()
המינון היומי של האם (לפי משטר מינון של 60 מ”ג/יום) הינו:
![]()
ומכאן מתקבל ה-RID:
![]()
על פי החישוב הנ”ל, החשיפה של התינוק לתרופה החדשה עוד יותר נמוכה מאשר לסרטרלין, ולכן עשויה להיות בטוחה יותר עבור התינוק. עם זאת, זהו שיקול אחד מתוך מכלול השיקולים שצריכים להנחות את המטפל בבואו להמליץ על טיפול תרופתי למטופלת, ויש להעריך בנוסף את יעילות התרופה עבור המטופלת עצמה, פרופיל תופעות לוואי וכו’.
מרכזי ייעוץ תרופתי בהיריון והנקה בארץ ובעולם
בישראל:
(בצפייה בטלפון נייד ניתן ללחוץ על מספר הטלפון לחיוג אוטומטי למספר):
- המרכז הארצי לייעוץ טרטולוגי של משרד הבריאות – 02-5082825
- היחידה לפרמקולוגיה קלינית וטוקסיקולוגיה במרכז הרפואי “שמיר” (הריופון) – 08-9779309
- המכון הארצי למידע בהרעלות – 04-7771900
- מרפאה טרטולוגית – ייעוץ תרופתי לנשים הרות במרכז הרפואי תל השומר – 03-5303168 (פקס)
בעולם:
- MotherToBaby – מרכז ייעוץ אמריקאי, המשוייך לארגון OTIS. האתר מכיל חומר עיוני רב הן למטופלות והן לאנשי מקצוע.
- Infantrisk Center – מרכז ייעוץ אמריקאי נוסף, המתמקד בייעוץ תרופתי בהנקה. באתר פועל גם פורום מקצועי שבו ניתן מענה לשאלות על ידי צוות המרכז. ניתן לחפש שאלות בנושאים מסויימים ואף לפרסם שאלה ישירות.
- UKTIS – מרכז ייעוץ תרופתי בריטי. האתר מכיל תקצירים בנושא מידע תרופתי בהיריון בלבד.
- Le Centre de Référence sur les Agents Tératogènes (CRAT) – מרכז ייעוץ תרופתי בשפה הצרפתית. מכיל מונוגרפים של תרופות רבות וכן מאפשר חיפוש לפי קבוצות פרמקולוגיות.
- Embryotox – מרכז ייעוץ תרופתי בשפה הגרמנית. האתר מכיל מונוגרפים רבים זמינים לכל. קיימת גם אפליקציה לנייד לאנדרואיד ולאייפון.
מקורות
Bolat, E., Bestas, A., Bayar, M. K., Ozcan, S., Erhan, O. L., & Ustundag, B. (2014). Evaluation of levobupivacaine passage to breast milk following epidural anesthesia for cesarean delivery. International Journal of Obstetric Anesthesia, 23(3), 217–221. https://doi.org/10.1016/j.ijoa.2014.03.005
Drugs and Lactation Database (LactMed) [Internet]. Bethesda (MD): National Library of Medicine (US); 2006-. Available from: https://www.ncbi.nlm.nih.gov/books/NBK501922/
Hale, T. W. (2019). Hale’s medications & Mothers’ milk, 2019: A Manual Of Lactational pharmacology. Springer Publishing Company.
Kelsey, J.J. (2016). Drug Principles in Lactation. Available at: https://www.accp.com/docs/bookstore/psap/p2016b3_sample.pdf
Neville, M. C. (1999). Physiology of lactation. Clinics in Perinatology, 26(2), 251–279. https://doi.org/10.1016/s0095-5108(18)30053-8
Villegas, L. R., Rivard, C. J., Hunter, B., You, Z., Roncal, C., Joy, M. S., & Le, M. P. T. (2018). Effects of fructose-containing sweeteners on fructose intestinal, hepatic, and oral bioavailability in dual-catheterized rats. PLOS ONE, 13(11). https://doi.org/10.1371/journal.pone.0207024
